Proč je důležité stimulovat bloudivý nerv při rakovině
Metaanalýza (bloudivý nerv – zánět – rakovina – variabilita srdečního rytmu HRV)
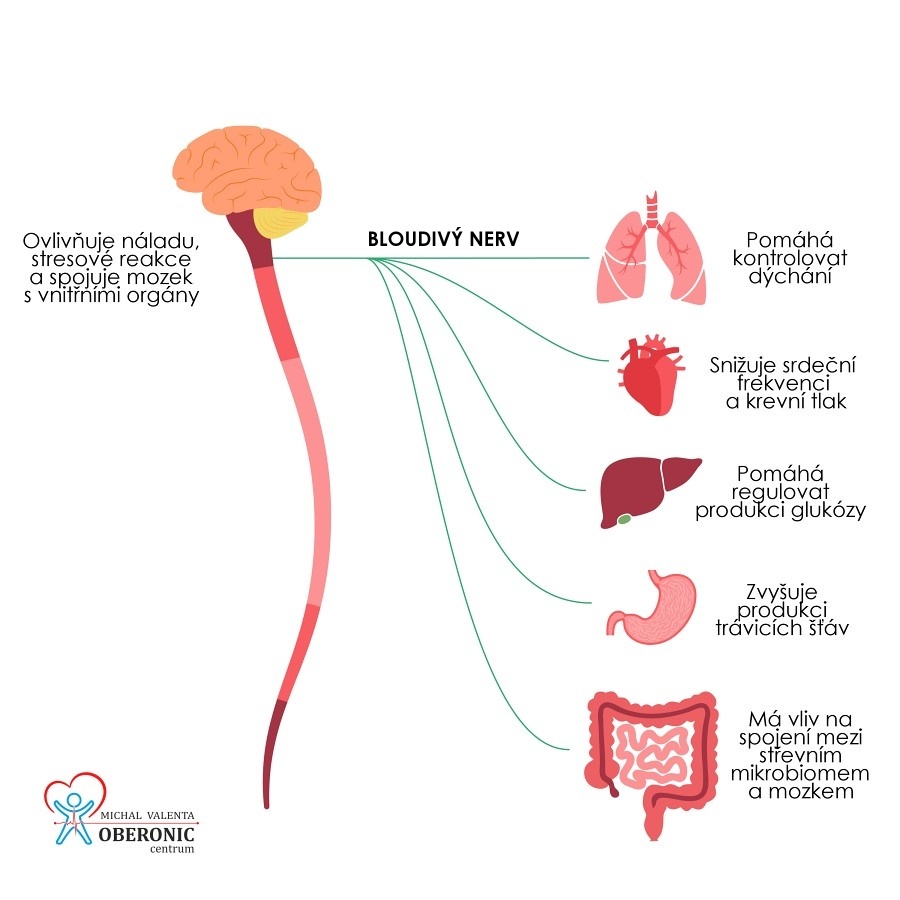
Když jsem nedávno našel tuto zajímavou metaanalýzu o prospěšnosti stimulace bloudivého nervu při rakovině, opět jsem si uvědomil jakou klíčovou funkci má bloudivý nerv při vyléčení z jakékoliv nemoci. Vzpomněl jsem si na různá „zázračná“ uzdravení, při nichž právě „on“ mohl hrát důležitou a významnou roli. Dnes už je zřejmé, že čím více je nemocný člověk v klidu, relaxaci, přijímá věci tak jak jsou, uvědomuje si sám sebe i proč nemoc přišla a pracuje na více úrovních svého bytí, většinou to zvládne a dojde k uzdravení. Toto je přesně mód kdy je bloudivý nerv aktivní a pracuje na plné obrátky, protože ho nepotlačuje žádný stres, strach, vztek, napětí, myšlenky „proč zrovna já“, zánět, další přidružené nemoci a dokáže organismu pomoci právě ve chvílích, kdy to nejvíce potřebuje. Aktivuje v těle velmi důležité „relaxační reakce“ a souhrou dalších regulačních systému napomáhá organismu k vyléčení. Tato metaanalýza (přeložená níže) nejenom vědecky dokládá přínos stimulace bloudivého nervu u rakoviny, ale otvírá i další témata, kterým se primárně věnuji na tomto webu. Je to především metoda analýzy variability srdeční frekvence (HRV) a propojení celku psycho-neuro-endokrino-imunitního systému. / M.V.
Souhrn metaanalýzy
U metastazujícího nádorového onemocnění se často vyskytuje únava, bolesti, úzkost, deprese, nespavost a poruchy kognitivních funkcí. Společného jmenovatele těchto příznaků lze vysvětlit poměrně logickým faktorem, a to nadměrným zánětem, který rovněž přispívá i k vzniku nádoru (tumorigeneze). Nejnovější výzkumy prokazují, že bloudivý nerv má protizánětlivou roli a ochranné účinky proti těmto příznakům a prognóze u různých druhů rakoviny. Zpočátku vysoká aktivita bloudivého nervu nezávisle předpovídá lepší prognózu rakoviny, konkrétně v metastatickém stadiu, a zmírňuje tyto příznaky.
Různé (polo)experimentální studie u lidí a zvířat ukázaly, že vagotomie (chirurgické přetětí bloudivého nervu) urychluje růst nádoru, zatímco aktivace bloudivého nervu zlepšuje prognózu rakoviny. Vzhledem k tomu, že pacienti s rakovinou mají nízkou aktivitu bloudivého nervu, poukazují tyto skutečnosti na silnou potřebu aktivovat tento nerv – tím snížit soubor příznaků a prodloužit přežití prostřednictvím snížení zánětu. Tento článek odhaluje nervovou modulaci nádorů a navrhuje novou podpůrnou léčbu rakoviny, jež by zlepšila prognózu pacientů a kvalitu jejich života.
Neuroendokrinně-imunitní model komorbidit a rakoviny
Pacienti s rakovinou mají při tomto onemocnění většinou přidružené problémy např. výskyt únavy, bolesti, úzkosti, deprese, nespavost a kognitivní poruchy. To vše ukazuje na společný etiologický rys, který lze vysvětlit neuroendokrinně-imunitním modelem. [8]. Tento model uvádí, že tyto příznaky jsou způsobeny především nadměrným zánětem. Řada studií také předkládá, že dalšími společnými rysy jsou nadměrná aktivita sympatického nervového systému (SNS) a zvýšený oxidační stres [9,10]. Toto krátké sdělení se však zaměří na zánět.
Opravdu v průběhu nádorového onemocnění dochází k masivní produkci cirkulujících cytokinů, které jsou součástí systémové bolesti, kterou pacienti s rakovinou pociťují [8], v souvislosti s únavou, úzkostí, depresí a nespavostí [11,12]. Důležité je, že nadměrný zánět je na jedné straně způsoben nádorem a na druhé straně konvenční léčbou, jako je chemoterapie a radioterapie [13]. Ačkoli jsou tyto léčebné postupy úspěšné, studie ukazují, že vyvolávají zvýšení hladiny zánětlivých cytokinů, které korelují s únavou [11], bolestí [14] a depresí [12].
Léčba může prostřednictvím zánětlivých procesů ovlivňovat také kognitivní funkce. Například zánět vyvolaný rakovinou a chemoterapií může zvýšit hladinu cytokinů (např. IL-6), jež se mohou dostat do mozku a stimulovat buňky k produkci dalších prozánětlivých cytokinů. Deregulace tak může vést k poškození DNA a narušení kognitivních funkcí [15]. Proto by tato „skupina příznaků“, jako je nespavost a kognitivní poruchy mohly být závažnější během aktivní léčby. Na druhou stranu tyto tři mechanismy (SNS, oxidační stres a zánět) a zvláště zánět přispívají k nádorovému bujení, neboť zánětlivá reakce hraje klíčovou roli a přispívá k úniku před apoptózou, angiogenezí a metastazováním [16-18].
Bloudivý nerv jako ochranný faktor
Nalezení nové, vědecky podložené léčby, která by se zaměřila na tento etiologický faktor (a zároveň na oxidační stres a nadměrnou aktivitu sympatiku), může tyto příznaky a prognózu zlepšit. Nejnovější výzkumy ukazují, že bloudivý nerv může mít ochranné účinky u různých druhů rakoviny. Bloudivý nerv je hlavním nervem parasympatického nervového systému a hraje důležitou roli u řady onemocnění, včetně rakoviny [19]. Tento nerv inhibuje (snižuje) oxidační stres, silně potlačuje zánět [20] a aktivitu sympatického nervového systému, což jsou tři mechanismy, jež můžou pomáhat při rakovině a dalších přidružených problémech [21].
Bylo prokázáno, že stimulace parasympatického nervového systému (prostřednictvím bloudivého nervu) vede ke snížení produkce prozánětlivých cytokinů prostřednictvím uvolňování neurotransmiteru acetylcholinu [20,22]. Bloudivý (vagový) nerv informuje mozek o nádorech a moduluje je prostřednictvím zpětné vazby na neuroendokrinní a imunitní systém [23]. Parasympatická nervová aktivita se obvykle měří pomocí analýzy variability srdeční frekvence (HRV), což je změna časových intervalů mezi jednotlivými po sobě jdoucími srdečními údery, jenž se měří na EKG [24]. Snížená HRV odráží nízkou aktivitu bloudivého nervu.
Vztah mezi HRV a prognózou
Bloudivý nerv zpomaluje nádorové bujení prostřednictvím inhibice prozánětlivých cytokinů [10,24,25]. Dále se ukázalo, že index aktivity bloudivého nervu, analyzován variabilitou srdeční frekvence (HRV), je u pacientů s rakovinou výrazně nižší než u zdravých lidí (HRV=20 vs. 50, p<0,001), a to konkrétně v metastatických stadiích. Kromě toho, náš tým prokázal, že vysoká aktivita bloudivého nervu předpovídala menší nádorovou zátěž a delší dobu přežití u několika typů rakoviny, jako je nemalobuněčný karcinom plic, prostaty, slinivky břišní a tlustého střeva, nezávisle na vedlejších faktorech [10,26,27], což potvrdily i další týmy ve svých studiích karcinomu prsu a dalších typů rakoviny [19,28].
Spiegelův tým prokázal že vyšší aktivita bloudivého nervu u pacientů s metastatickým nebo recidivujícím karcinomem prsu významně předpovídala delší dobu přežití [29]. Náš tým dále prokázal, že HRV velmi silně predikuje nádorovou zátěž, a to zejména u pacientů s metastazujícím karcinomem [10].
V jiné studii jsme poprvé prokázali prognostickou hodnotu nového komplexního biomarkeru, který odráží autonomní a imunitní systém, ve vztahu k prognóze nádorových onemocnění. Dvě studie odhalily, že nový index neuroimunomodulace (NIM), jenž odráží aktivitu bloudivého nervu a měří se při analýze HRV – tzv. střední kvadratická odchylka po sobě jdoucích RR intervalů (RMSSD), významně předpovídal celkové přežití u pacientů s pokročilou rakovinou slinivky břišní a u pacientů s nemalobuněčným karcinomem plic, oproti celkovému indexu systémového zánětu (CRP). Pacienti s nemalobuněčným karcinomem plic a relativně vysokým indexem NIM měli téměř dvojnásobnou dobu přežití ve srovnání s pacienty s nízkým indexem NIM [31].
Vztah mezi HRV a příznaky
Kromě negativního vlivu nízké HRV na nádorové onemocnění studie prokázaly přímý vztah mezi nízkou HRV a únavou, bolestí, úzkostí, depresí, nespavostí a kognitivními poruchami. Byla prokázána souvislost mezi nižší parasympatickou aktivitou a vyšší mírou únavy u osob, které přežily rakovinu prsu [32], přičemž některé studie ukazují, že zprostředkujícím faktorem je zánět.
Dva přehledy a metaanalýzy ukázaly, že HRV je u osob s těžkou depresí významně nižší než u osob bez deprese [33]. Jiná metaanalýza ukázala, že pacienti s chronickou bolestí mají sníženou HRV ve srovnání se zdravými lidmi a že experimentálně vyvolaná bolest u zdravých lidí HRV dokonce snižuje [34].
Studie u pacientů s rakovinou ukázala, že pacienti s depresí a úzkostí z operace mají významně sníženou HRV ve srovnání s pacienty bez deprese a úzkosti [35]. Při zkoumání specifických aspektů QOL (quality of live-kvality života) souvisejících s nádorovým onemocněním je aktivita bloudivého nervu nepřímo úměrná bolesti (r = -0,46, p < 0,05) a jeho aktivita a vysoký tonus může bolest snižovat [14]. Nízká HRV také nepřímo souvisí s poruchami spánku, kognitivními poruchami a pocitem beznaděje [36,37]. V neposlední řadě se aktivita bloudivého nervu podílí také na autoregulaci emocí a sociální aktivity [38] a je spojena s dodržováním léčby u rakoviny prsu.
Stimulace vagového nervu
Bloudivý nerv lze stimulovat farmakologicky, invazivně i neinvazivně. Přístroj (implantát) pro stimulaci bloudivého nervu (VNS – Vagus Nerve Stimulation) je již více než 10 let schválen FDA (úřad pro kontrolu potravin a léčiv) pro léčbu epilepsie a v současné době probíhají klinické studie pro léčbu rezistentní deprese [40]. Přímá elektrická stimulace bloudivého nervu také tlumí produkci TNFα během experimentálních modelů endotoxémie (onemocnění gastrointestinálního traktu), hemoragického šoku a dalších stavů nadbytku cytokinů [41].
Kromě toho existují i některé neinvazivní techniky stimulace bloudivého nervu. Bylo prokázáno, že transkutánní stimulace vagového nervu (t-VNS) (Gammacore a Cerbomed) snižuje hladiny zánětlivého mediátoru High Mobility Group Box 1 (HMGB1) a zlepšuje přežití na modelu myší sepse [42]. V nedávné studii bylo také zjištěno, že nový přístroj t-VNS snižuje různé zánětlivé markery u lidí [43] a ve dvou nedávných studiích na lidech snižuje depresi o 50 % [44]. Dále bylo zjištěno, že tVNS snižuje bolesti hlavy u pacientů s chronickou migrénou [45].
Studie také prokázaly, že více forem meditace může změnit parasympatickou složku – zvýšit HRV a může mít pozitivní vliv na srdeční autonomní tonus [46]. Podobně relaxační terapie a HRV biofeedback, což jsou behaviorální metody, mohou významně
zvýšit parasympatickou složku a HRV, což odráží zvýšení aktivity bloudivého nervu [47].
Dále byly vyvinuty některé terapeutické látky zaměřené na cholinergní protizánětlivou dráhu prostřednictvím působení na bloudivý nerv. Příkladem je protizánětlivá látka GTS-21 a CNI- 1493, nazývaný také semapimod, což je lék působící prostřednictvím intaktního bloudivého nervu. Po podání semapimodu byla pozorována zvýšená aktivita eferentního bloudivého nervu, což dokazuje jeho aktivační potenciál [48]. Pouze dvě studie zkoumaly účinky semapimodu a jedna pilotní studie účinky HRV-Biofeedbacku přímo na rakovinu. [49] Zkoumala účinky CNI-1493 a při porovnání objemu nádorů v kontrolní skupině a ve skupině, která dostávala CNI-1493, byl zjištěn menší objem nádoru než u druhé skupiny (i když to statisticky netestovali) [50]. Na druhé straně ukázali, že aktivace bloudivého nervu pomocí semapimodu snižuje metastazování myšího karcinomu prsu.
Nedávná matched- controlled pilotní studie naší skupiny (De Couck et al. submitted) ukázala pozitivní účinky HRV-Biofeedbacku (HRV-B) u pacientů s metastazujícím karcinomem tlustého střeva. Zatímco u kontrolní skupiny se hladina karcinoembryonálního antigenu (CEA) téměř nezměnila, pacienti provádějící HRV-B vykazovali zřetelný prudký pokles hladiny CEA, která po třech měsících měla tendenci být významně nižší než u kontrolní skupiny (p<0,06) (De Coucket al., submitted).
Tato velká metaanalýza vyšla v časopise Clinics in Oncology (nejuznávanější platforma pro šíření klinického onkologického výzkumu mezi čtenáři).
Více informací o neinvazivní stimulaci bloudivého nervu zde: 13 způsobů přirozené stimulace bloudivého nervu
Metaanalýza: Why we Should Stimulate the Vagus Nerve in Cancer
Překlad: Centrum Oberonic
M.V.
Reference:
et al. Health related quality of life outcomes in cancer clinical trials. Eur J
Cancer. 2005;41(12):1697-709.
2. Chida Y, Steptoe A. Positive psychological well-being and mortality: a
quantitative review of prospective observational studies. Psychosom Med.
2008;70(7):741-56.
3. Andrykowski MA, Schmidt JE, Salsman JM, Beacham AO, Jacobsen
PB. Use of a case definition approach to identify cancer-related fatigue
in women undergoing adjuvant therapy for breast cancer. J Clin Oncol.
2005;23(27):6613-22.
4. Palesh OG, Roscoe JA, Mustian KM, Roth T, Savard J, Ancoli-Israel S,
et al. Prevalence, demographics, and psychological associations of sleep
disruption in patients with cancer: University of Rochester Cancer Center-
Community Clinical Oncology Program. J Clin Oncol. 2010;28(2):292-8.
5. Jim HS, Phillips KM, Chait S, Faul LA, Popa MA, Lee Y-H, et al. Metaanalysis
of cognitive functioning in breast cancer survivors previously
treated with standard-dose chemotherapy. J Clin Oncol. 2012;30(29):3578-
87.
6. Redeker NS, Lev EL, Ruggiero J. Insomnia, fatigue, anxiety, depression,
and quality of life of cancer patients undergoing chemotherapy. Sch Inq
Nurs Pract. 2000;14(4):275-90.
7. Montazeri A. Health-related quality of life in breast cancer patients: a
bibliographic review of the literature from 1974 to 2007. J Exp Clin Cancer
Res. 2008;27:32.
8. Miller AH, Ancoli-Israel S, Bower JE, Capuron L, Irwin MR. Neuro
endocrine-immune mechanisms of behavioral comorbidities in patients
with cancer. J Clin Oncol. 2008;26(6):971-82.
9. Panis C, Pavanelli WR. Cytokines as Mediators of Pain-Related Process in
Breast Cancer. Mediators Inflamm. 2015;129034.
10. De Couck M, Gidron Y. Norms of vagal nerve activity, indexed by Heart
Rate Variability, in cancer patients. Cancer Epidemiol. 2013;37(5):737-41.
11. Schubert C, Hong S, Natarajan L, Mills PJ, Dimsdale JE. The association
between fatigue and inflammatory marker levels in cancer patients: a
quantitative review. Brain Behav Immun. 2007;21(4):413-27.
12. Haberkorn J, Burbaum C, Fritzsche K, Geser W, Fuchs D, Ocaña-Peinado
FM, et al. Day-to-day cause-effect relations between cellular immune
activity, fatigue and mood in a patientwith prior breast cancer and current
cancer-related fatigue and depression. Psychoneuroendocrinology.
2013;38(10):2366-72.
13. Vyas D, Laput G, Vyas AK. Chemotherapy-enhanced inflammation
may lead to the failure of therapy and metastasis. Onco Targets Ther.
2014;7:1015-23.
14. De Couck M, Nijs J, Gidron Y. You may need a nerve to treat pain: the
neurobiological rationale for vagal nerve activation in pain management.
Clin J Pain. 2014;30(12):1099-105.
15. Loh KP, Janelsins MC, Mohile SG, Holmes HM, Hsu T, Inouye SK, et al.
Chemotherapy-related cognitive impairment in older patients with cancer.
J Geriatr Oncol. 2016;7(4):270-80.
16. Mantovani A, Allavena P, Sica A, Balkwill F. Cancer-related
inflammation. Nature. 2008;454(7203):436-44.
17. Pikarsky E, Porat RM, Stein I, Abramovitch R, Amit S, Kasem S, et al.
NF-kappaB functions as a tumour promoter in inflammation-associated
cancer. Nature. 2004;431(7007):461-6.
18. Voronov E, Shouval DS, Krelin Y, Cagnano E, Benharroch D, Iwakura Y,
et al. IL-1 is required for tumor invasiveness and angiogenesis. Proc Natl
Acad Sci. 2003;100(5):2645-50.
19. De Couck M, Caers R, Spiegel D, Gidron Y. The role of the vagus nerve
in cancer prognosis: A comprehensive review. Journal of Oncology.
2018:1236787.
20. Tracey KJ. Reflex control of immunity. Nat Rev Immunol. 2009;9:418-28.
21. De Couck M, van Brummelen D, Schallier D, De Grève J, Gidron Y. The
relationship between vagal nerve activity and clinical outcomes in prostate
and non-small cell lung cancer patients. Oncol Rep. 2013;30(5):2435-41.
22. Tracey KJ. The inflammatory reflex. Nature. 2002;420(6917):853-9.
23. Heart rate variability: standards of measurement, physiological
interpretation and clinical use. Task Force of the European Society
of Cardiology and the North American Society of Pacing and
Electrophysiology. Circulation. 1996;;93(5):1043-65.
24. Gidron Y, Perry H, Glennie M. The vagus may in form the brain about
sub-clinical tumors and modulate them: an Hypothesis. Lancet Oncol.
2005;6:245-8.
25. De Couck M, Mravec B, Gidron Y. You may need the vagus nerve
to understand pathophysiology and to treat diseases. Clin Sci.
2012;122(7):323-8.
26. De Couck M, Maréchal R, Moorthamers S, Van Laethem JL, Gidron Y.
Vagal nerve activity predicts overall survival in metastatic pancreatic
cancer, mediated by inflammation. Cancer Epidemiol. 2016;40:47-51.
27. Mouton C, Ronson A, Razavi D, Delhaye F, Kupper N, Paesmans M,
et al. The relationship between heart rate variability and time-course
of carcinoembryonic antigen in colorectal cancer. Auton Neurosci.
2012;166(1-2):96-9.
28. Zhou X, Ma Z, Zhang L, Zhou S, Wang J, Wang B, et al. Heart rate variability
in the prediction of survival in patients with cancer: A systematic review
and meta-analysis. J Psychosom Res. 2016;89:20-5.
29. Giese-Davis J, Wilhelm FH, Tamagawa R, Palesh O, Neri E, Taylor CB,
et al. Higher vagal activity as related to survival in patients with advanced
breast cancer: an analysis of autonomic dysregulation. Psychosom Med.
2015;77(4):346-55.
30. Gidron Y, De Couck M, De Greve J. If you have an active vagus nerve,
cancer stage may no longer be important. J Biol Regul Homeost Agents.
2014;28(2):195-201.
31. Gidron Y, De Couck M, Schallier D, De Greve J, Van Laethem JL, Maréchal
R. The Relationship between a New Biomarker of Vagal Neuroimmuno
modulation and Survival in Two Fatal Cancers. J Immunological Res.
2018:4874193.
32. Crosswell AD, Lockwood KG, Ganz PA, Bower JE. Low heart rate
variability and cancer-related fatigue in breast cancer survivors.
Psychoneuroendocrinology. 2014;45:58-66.
33. Huang M, Shah A, Su S, Goldberg J, Lampert RJ, Levantsevych OM, et
al. Association of Depressive Symptoms and Heart Rate Variability in
Vietnam War-Era Twins: A Longitudinal Twin Difference Study. JAMA
Psychiatry. 2018;75(7):705-12.
34. Koenig J, Falvay D, Clamor A, Wagner J, Jarczok MN, Ellis RJ, et al.
Pneumogastric (Vagus) Nerve Activity Indexed by Heart Rate Variability
in Chronic Pain Patients Compared to Healthy Controls: A Systematic
Review and Meta-Analysis. Pain Physician. 2016;19(1):E55-78.
35. Kim EH, Park JH, Lee SM, Gwak MS, Kim GS, Kim MH. Preoperative
depressed mood and perioperative heart rate variability in patients with
hepatic cancer. J Clin Anesth. 2016;35:332-338.
36. Hovland A, Pallesen S, Hammar A, Hansen AL, Thayer JF, Sivertsen B, et
al. Subjective sleep quality in relation to inhibition and heart rate variability
in patients with panic disorder. J Affect Disord. 2013;150(1):152-5.
37. Schwarz AM, Schächinger H, Adler RH, Goetz SM. Hopelessness is
associated with decreased heart rate variability during championship chess
games. Psychosom Med. 2003;65(4):658-61.
38. Thayer JF, Ahs F, Fredrikson M, Sollers JJ 3rd, Wager TD. A meta-analysis
of heart rate variability and neuro imaging studies: implications for heart
rate variability as a marker of stress and health. Neuro sci Biobehav Rev.
2012;36(2):747–56.
39. Karvinen K, Murray N, Arastu H, Allison R. Stress reactivity, health
behaviors, and compliance to medical care in breast cancer survivors.
Oncol Nurs Forum. 2013;40(2):149-56.
40. Corcoran C, Connor TJ, O’Keane V, Garland MR. The effects of vagus
nervestimulation on pro- and anti-inflammatory cytokines in humans: a
preliminary report. Neuroimmunomodulation. 2005;12(5):307-9.
41. Borovikova LV, Ivanova S, Zhang M, Yang H, Botchkina GI, Watkins
LR, et al. Vagus nerve stimulation attenuates the systemic inflammatory
response to endotoxin. Nature. 2000;405(6785):458-62.
42. Huston JM, Gallowitsch-Puerta M, Ochani M, Ochani K, Yuan R, Rosas-
Ballina M, et al. Transcutaneous vagus nerve stimulation reduces serum
high mobility group box 1 levels and improves survival in murine sepsis.
Crit Care Med. 2007;35(12):2762-8.
43. Brock C, Brock B, Aziz Q, Møller HJ, Pfeiffer Jensen M, Drewes AM, et
al. Transcutaneous cervical vagal nervestimulation modulates cardiac
vagal tone and tumor necrosis factor-alpha. Neurogastroenterol Motil.
2017;29(5).
44. Hein E, Nowak M, Kiess O, Biermann T, Bayerlein K, Kornhuber J, et al.
Auricular transcutaneous electrical nerve stimulation in depressed patients:
a randomized controlled pilot study. J Neural Transm. 2013;120(5):821-7.
45. Silberstein SD, Mechtler LL, Kudrow DB, Calhoun AH, McClure C, Saper
JR, et al. Non-invasive vagus nerve stimulation for the acute treatment
of cluster headache: findings from the randomized, double-blind, shamcontrolled
ACT1 study. Headache. 2016;56(8):1317-32.
46. Paul-Labrador M, Polk D, Dwyer JH, Velasquez I, Nidich S, Rainforth M,
et al. Effects of a randomized controlled trial of transcendental meditation
on components of the metabolic syndrome in subjects with coronary heart
disease. Arch Intern Med. 2006;166(11):1218-24.
47. Sakakibara M, Hayano J, Oikawa LO, Katsamanis M, Lehrer P. Heart
rate variability biofeedback improves cardio respiratory resting function
during sleep. Appl Psychophysiol Biofeedback. 2013;38(4):265-71.
48. Pavlov VA, Ochani M, Gallowitsch-Puerta M, Ochani K, Huston JM,
Czura CJ, et al. Central muscarinic cholinergic regulation of the systemic
inflammatory response during endotoxemia. Proc Natl Acad Sci U S A.
2006;103(13):5219-23.
49. Kemeny MM, Botchkina GI, Ochani M, Bianchi M, Urmacher C, Tracey
KJ. The tetravalent guanylhydrazone CNI-1493 blocks the toxic effects of
interleukin-2 without diminishing antitumor efficacy. Proc Natl Acad Sci
U S A. 1998;95(8):4561-6.
50. Erin N, Duymuş O, Oztürk S, Demir N. Activation of vagus nerve by
semapimod alters substance P levels and decreases breast cancer metastasis.
Regul Pept. 2012;179(1-3):101-8.
51. Kim W, Youn H, Kang C, Youn B. Inflammation-induced radio resistance
is mediated by ROS-dependent
52. inactivation of protein phosphatase 1 in non-small cell lung cancer cells.
Apoptosis. 2015;20(9):1242-52.
53. Sultani M, Stringer AM, Bowen JM, Gibson RJ. Anti-Inflammatory
Cytokines: Important Immunoregulatory Factors Contributing to
Chemotherapy-Induced Gastrointestinal Mucositis. Chemother Res Pract.
2012;490804.
Analyzuje mnoho tělesných systémů a paramentů organismu, mimo jiné i aktivitu bloudivého nervu.
⇐ Koenzym Q10 (Ubiquinol) je vyroben pokročilou patentovanou technologií, která zaručuje vysokou stabilitu, absorpci a tím i lepší účinky.
⇒ BrainMax Adaptogenic nejvíce prozkoumané adaptogeny z celého světa, jež pozitivně ovlivňují činnost unavených nadledvinek, zvyšují odolnost na psychický i fyzický stres a pomáhají s nedostatkem energie a únavou.




